Arranjo Experimental
A célula de eletrodeposição consiste em um recipiente de vidro com diâmetro aproximado de $5\,\text{cm}$ e profundidade de cerca de $1\,\text{cm}$. Este é preenchido com uma solução aquosa de $\text{ZnCl}_2$ $0{,}1\,\text{M}$ até uma profundidade de $0{,}5\,\text{cm}$. Embora a literatura frequentemente cite a adição cuidadosa de acetato de butila ($\text{CH}_3\text{COO}(\text{CH}_2)_3\text{CH}_3$) para a formação de uma interface líquido-líquido, optou-se, neste trabalho, por realizar a deposição sobre papel de filtro para viabilizar a análise por Microscopia Eletrônica de Varredura (MEV).
Um cátodo de carbono (mina de grafite com diâmetro de $0{,}5\,\text{mm}$) foi polido cuidadosamente para se obter uma superfície plana e perpendicular ao eixo do eletrodo. Em seguida, o cátodo foi posicionado no centro do recipiente, de modo que sua extremidade plana permanecesse exatamente sobre o papel. O eletrodo de carbono foi imerso na solução de cloreto de zinco e conectou-se a uma fonte de corrente contínua. Aplicou-se uma diferença de potencial constante de $9\,\text{V}$, fazendo com que o eletrodo atuasse como cátodo. Nessas condições, ocorre a redução e deposição de zinco metálico na sua extremidade. O procedimento é análogo ao realizado anteriormente com o cobre ($Cu$). O experimento foi conduzido à temperatura ambiente ($27\,^\circ\text{C}$).
O processo baseia-se em reações de oxirredução, nas quais a redução de cátions metálicos ($\text{M}^{y+}$) na interface do cátodo resulta em depósitos sólidos estáveis com geometrias fractais. Uma folha metálica de zinco cresce bidimensionalmente no papel, a partir da borda da extremidade plana do cátodo em direção ao ânodo externo. Alguns minutos após o início do experimento, os prolongamentos ramificados tornam-se perceptíveis. O crescimento foi interrompido (desligando-se a fonte) assim que um dos ramos atingiu $2\,\text{cm}$ de distância do cátodo. A manipulação de variáveis operacionais (tensão, concentração e material do eletrodo) permite o controle morfológico dos cristais, tornando este experimento uma ferramenta didática vantajosa em comparação à eletrólise convencional da água ou de cloretos.

(foto: nelson)
Resultados e Discussão
A eletrodeposição quase-bidimensional é um sistema-modelo ideal para o estudo dessas estruturas devido ao facilidade de controle experimental. Historicamente, sabe-se que a morfologia depende do ambiente físico-químico na interface de crescimento. Este sistema permite a observação direta da nucleação e do crescimento de sólidos metálicos em tempo real. Neste experimento, a deposição de $\text{Zn}$ ocorre de tal maneira que se forma um depósito metálico fractal na superfície do papel.
Em diversos ambientes naturais, os processos de difusão e agregação frequentemente dominam o transporte de partículas ou moléculas. De modo análogo, nesse sistema eletroquímico, forma-se uma “árvore de zinco”, apresentando estruturas fractais geradas pelo processo de agregação. Por exemplo, uma árvore botânica é um fractal natural, pois, se um de seus galhos for quebrado, ele se assemelhará à árvore inteira em miniatura (autossimilaridade).
A morfologia resultante é uma função direta da densidade de corrente (tensão aplicada) e da concentração iônica, onde o equilíbrio entre a taxa de nucleação e a taxa de crescimento determina a estética e compactação do depósito.
A seguir, são apresentados os resultados das análises por microscopia óptica e fotografia digital, utilizadas para o estudo dos padrões de crescimento, e por Microscopia Eletrônica de Varredura (MEV), empregada para a análise morfológica e de textura dos depósitos.

(foto: graziela)
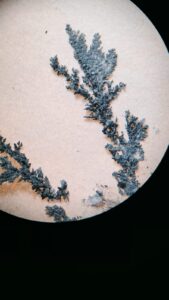
(foto: graziela)

(imagem MEV: Thales/ CEMIC-Unifal-MG)

